Моноцитарный эрлихиоз у собак (Еhrlichia Canis Infection)

Еще фото
Автор (ы): Цачев И.Ц., DVM, MSc, PhD, DSc Департамент микробиологии, инфекционных и паразитарных болезней, Факультет ветеринарной медицины государственного Тракийского университета, г. Стара Загора, Болгария, Димов И.Д., DVM, MSc, Учреждение Академии наук России, г.Санкт-Петербург
Журнал: №5 - 2011
Еhrlichia canis инфекция, переносчиком которой являются клещи, и которая, в своем клиническом проявлении известна как моноцитарный эрлихиоз у собак (МЭС). Возбудитель - рикетсия Ehrlichia canis.
Болезнь известна в мире еще и под названиями Canine rickettsiosis, Canine hemorrhagic fever, Tracker dog disease, Canine tick typhus, Nairobi bleeding disorder и Tropical canine pancytopenia.
История и распространение
Впервые эрлихиоз у собак был доказан в Алжире в 1935 году (Donatein и Lestoquard). Позже исследования Paul Ehrlich (1945) показали отличия новых организмов от других внутриклеточных агентов и в его честь их назвали эрлихиями. Во время войны во Вьетнаме (1968-1970 гг.) американские войска потеряли около 300 военных собак из-за этой новой и незнакомой болезни (Walker еt al.,1970; Huxsoll et al.,1970). Особое внимание уделяется эрлихиям с 1987 года, когда доказана их роль как возбудителей заболеваний у людей.
МЭС была доказана во многих странах Африки, Азии, Ближнего Востока, Европы и США. Данные о распространенности инфекции в мире показывают следующую картину: Тайвань - 9%, Бразилия - 23%, Египет - 33%, Иран - 38-67%, Зимбабве - 42%, Израиль - 63%, Турция - 74%. В США МЭС является вторым по распространенности инфекционным заболеванием (после парвовирусного энтерита).
Для Греции Е.canis самая встречаемая векторная инфекция у собак. В Польше Е.canis проявляется в первый раз в 2003 году (Płoneczka and Śmielewska-Łoś E). В 2004 году была выявлена и в Словакии (Letkova и сотр). Из 78 исследованных собак у 29 (37.2%) регистрируются антитела E.canis.
В Болгарии заболевание доказано первый раз в 2003 году. Установлена средняя серопревалентность - 34% E.canis в стране (Цачев, 2006).
Этиология
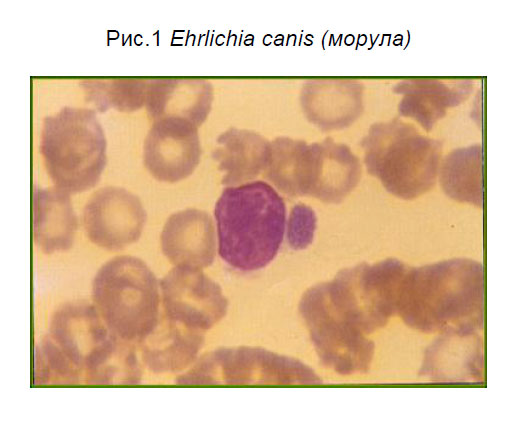
Эрлихии являются грамотрицательными, облигатными, внутриклеточными агентами. Их средний размер 0,5-1,5 μm. Паразитируют в плазме моноцитов в виде морул, которые окрашиваются в синий цвет по Романовски-Гимзе (Рис.1). Не содержат липополисахаридных эндотоксинов и липополисахарид в их клеточной стенке. Исследования эрлихий последних лет пролили новый свет на них и их классификацию.
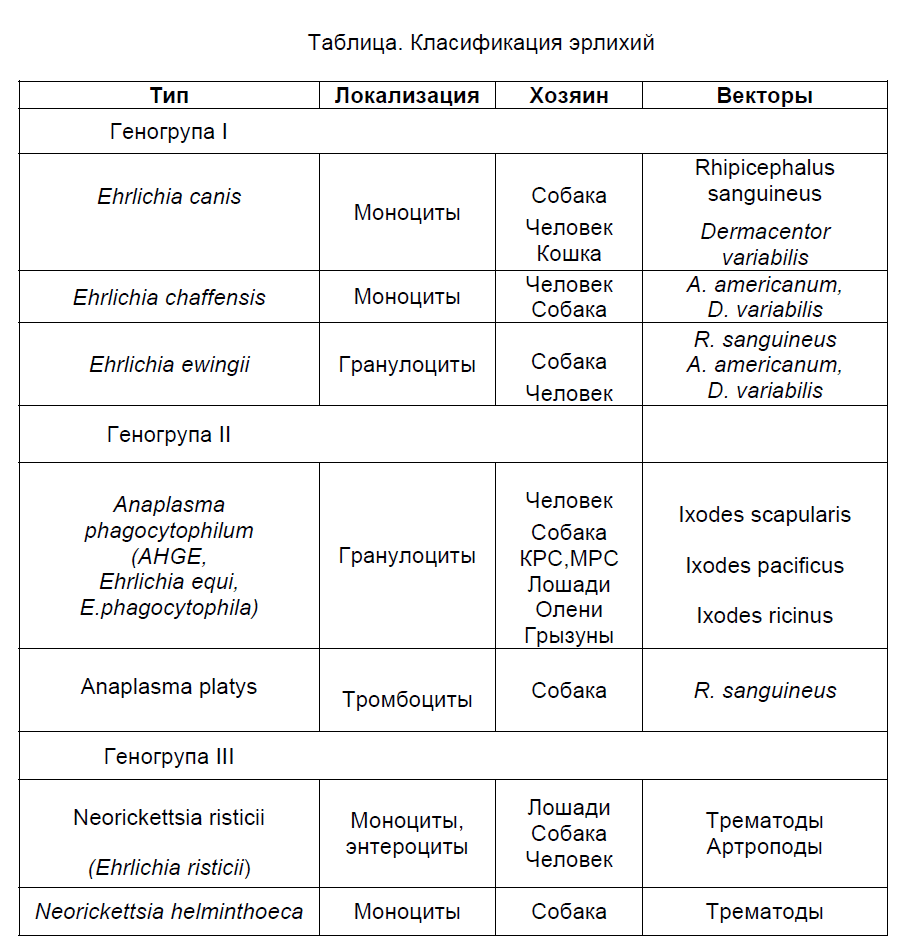
Последнее систематизирование эрлихий сделано на основе генетического анализа (16SrRNA генная секвенция) и классифицирует их в 3 генетически родственные группы (Табл.). Литературные данные показывают, что до сих пор выделены 3 штамма Е.canis, генетически охарактеризованые как: Florida stain (Gen Bank accession No M73226), Oklahoma strain /M73221/, Israeli strain (U26740).
E.canis можно культивировать в DH82 клеточной линии.
Эпизоотология
Источником инфекции у МЭС являются собаки с явной или скрытой формой заболевания. Заражение трансмиссивное – через посредничество клещей. Основным переносчиком E.canis является собачий клещ Rhipicephalus sanguineus. Заражение вектора происходит во время его жизненного цикла – в фазе личинки или нимфы, когда он питается кровью инфицированной собаки. Имаго также может заразиться и передать возбудителя каждый раз, во время питания кровью. Пока еще не наблюдалась трансовариальная передача эрлихий. Экспериментально установлено, что клещи могут выжить без пищи от 155 до 568 дней и, что они действуют как естественные резервуары до 155 дней после их заражения. Это явление позволяет клещам сохранить эрлихии с осени до весны. Как известно, векторы МЭС наиболее активны в теплые месяцы года, и это определяет сезонность данного заболевания.
Литературные данные не сообщают о существенных различиях в предрасположенности по возрасту и полу собак. Все породы могут заболеть, но наиболее распространено это заболевание, и с более тяжелыми осложнениями замечено у немецких овчарок.
Патогенез
Заболевание может протекать в острой, подострой и хронической форме. Во время острой фазы возбудители проникают в моноциты крови, реплицируются, а затем локализируются в мононуклеарные фагоцитарные клетки селезенки, печени и в лимфатические узлы. Затем происходит диссеминирование в эндотелиальных клетках других органов и систем, и развивается васкулит.
Экспериментально доказано появление IgA и IgМ антител после седьмого дня инфекции, а после четырнадцатого дня и появление IgG. Существуют доказательства участия иммунных механизмов в патогенезе заболевания. Например, плазматические клетки интенсивно инфильтрируют паренхиматозные органы; появляются периваскулярные инфильтраты в легких, почках, селезенке, мозговых оболочках и глазах; имеется наличие положительных антиглобулиновых и автоаглутинационных тестов; иммунопатологическая форма проявляется в появлении антитромбоцитарных антител; появляется гипергаммаглобулинемия, которая сохраняется на всех этапах. У собаки, кроме того, может развиться субклиническая инфекция, которая может сохраняться в течение месяцев или нескольких лет. Предполагается, что только иммунокомпетентные животные способны устранить возбудителя во время субклинической фазы. Субклиническая фаза может перейти в хроническую, которая может протекать иначе – от легкой к более тяжелой клинике со смертельным исходом. Причина смерти при МЭС часто является следствием массивной кровопотери.
Клиническая картина
Острая форма. Инкубационный период составляет от 1 до 3 недель. Вначале наблюдается депрессия, вялость, потеря веса и аппетита. У больных развивается лихорадка с четко выраженной лимфоаденомегалией и спленомегалией. Появляется кровотечение, в основном петехии и экхимозы на коже и слизистой оболочке, редко наблюдается эпистаксис. У больных собак иногда наблюдается рвота и развитие гнойно-катарального ринита. У некоторых животных развивается хромота, атаксия и одышка. Очень часто владельцы и врачи обнаруживают клещей на теле больной собаки.
Острое протекание может перейти в выздоровление без терапии или может перейти в субклиническую форму. Если организм не удалит возбудителя во время бессимптомной формы, может развиться хроническая форма.
Хроническая форма. При хроническом протекании болезни наблюдаются следующие, наиболее типичные клинические проявления: общая слабость, депрессия, потеря аппетита, потеря веса, усталость, бледные слизистые оболочки, лихорадка, гепатомегалия, отеки задних лап и мошонки. Наблюдаются кровоизлияния в коже и слизистых оболочках собаки. При проявлении вторичной микрофлоры (бактерии и простейшие), развивается интерстициальная пневмония, гломерулонефрит, почечная недостаточность и артрит. Хроническое развитие болезни часто приводит к репродуктивным расстройствам у пациентов – аномально длинный эстральный цикл, аборты, неонатальная смерть. Есть сообщения о полимиозите у собак.
Нервные симптомы наблюдались у МЭС как в острой, так и в хронической форме. Они связаны с менингоэнцефалитом (изгиб спины, боли в шее и спине), парезами, атаксией, судорогами. Эти признаки вызваны геморрагиями, васкулитом и периваскулярными инфильтратами в мозговых оболочках у пациентов.
В одной трети случаев затрагивается и зрительный аппарат. Появляется помутнение роговицы, передний увеит, фокальные хориоретинальные очаги, субретинальная геморрагия, которые часто приводят к слепоте.
Описанные признаки у МЭС во многом зависят от циркулирующего штамма. Важное значение имеет инфекционная доза, порода, иммунный статус хозяина и наличие других векторных возбудителей.
Патологоанатомическая картина
Типичные патологоанатомические изменения у МЭС включают в себя: петехии, экхимозы слизистых оболочек большинства органов, в том числе полости рта, легких, почек, мочевого пузыря, желудочно-кишечного тракта, плевры.
Спленомегалия, гепатомегалия и генерализованная лимфаденопатия часто выявляются при остром течении болезни. Увеличены лимфатические узлы в коричневом цвете. Костный мозг имеет красный цвет, он гиперпластический при остром протекании и гипопластический при хроническом протекании болезни. Ослабление и отставание в росте особенно существенно наблюдается в хроническом процессе.
Типичной гистологической находкой у МЭС является периваскулярная клеточная инфильтрация во многих органах и тканях – легких, мозгах, мозговых оболочках, почках, лимфатических узлах, костном мозге, селезенке, а иногда по коже и в слизистых оболочках. В центральной нервной системе развивается мультифокальный негнойный менингоэнцефалит. Легочные изменения - интерстициальная пневмония с субэндотелиальным накоплением мононуклеаров в сочетании с интерстициальным и альвеолярным кровоизлиянием. Нарушения функции почек включают васкулит, который сопровождается кортикомедулярной клеточной инфильтрацией и гломерулонефритом.
Диагностика
Диагностика МЭС основана на данных анамнеза, истории болезни, клинических и эпизоотологических обследований и, особенно, лабораторных исследований.
Гематология. Наиболее распространенными являются гематологические изменения: тромбоцитопения, нерегенеративная, нормоцитарная, нормохромная анемия и лейкопения. В субклинической форме также доказана тромбоцитопения. Развитие тяжелой панцитопении связано с затрагиванием костного мозга (Рис.2).
Биохимия. Гипоальбуминемия, гиперглобулинемия и гипергаммаглобулинемия часто встречаемые биохимические изменения при эрлихиозе. Стоит отметить, что гипергаммаглобулинемия не коррелирует с титром антител к Е.canis. Это указывает на наличие неспецифической антителопродукции, индуцированной эрлихиями и на то, что Е.canis – антитела не являются главной причиной увеличения в сыворотке крови гамма-глобулинов. Это явление известно и при других инфекционных заболеваниях и тесно связано с недостаточной эффективностью иммунного ответа. Энзимный профиль у МЭС до сих пор недостаточно изучен и данных по нему относительно мало. Есть данные о временном увеличении в сыворотке ALT и ALP.
Серология. В настоящее время наиболее используемым и предпочтительным методом для диагностики МЭС является непрямая иммунофлюоресценция (IFA) сыворотки крови. Метод определен как золотой стандарт (gold standart ) в диагностике заболевания. Титры выше 1:40/1:100 являются показателем инфекции в целом. При остром протекании заболевания серологические титры могут достигать очень высоких значений: от 1:5120 до 1:10240 или более в течение 8 недель после заражения. ELISA метод также принимается в МЭС, но в последнее время на рынке появились экспресс-диагностические комплекты (IDEXX).
Микроскопия. Обнаружение интрацитоплазматических морул Е.canis в моноцитах крови при остром течении МЭС является достаточным признаком для инфекции. Легко можно сделать мазок из крови, лейкомассы (buffy coat), лимфатических узлов или костного мозга для микроскопического исследования. Исследования из цельной крови таким способам доказывают наличия морул только у 4% из исследованных образцов.
Другие, менее широко используемые техники для диагностики, это - культивирование (занимает от 14 до 34 дней), ПЦР и Western immunoblotting, которые на данном этапе осуществляются только в специализированных научно-исследовательских лабораториях.
Дифференциальный диагноз
Включает в себя: гранулоцитарный анаплазмоз, болезнь Лайма, гепатозооноз, чума собак и другие заболевания.
Коинфекции
Векторные инфекции, переносчиками которых являются клещи: эрлихиоз, гепатозооноз, анаплазмоз, рикетсиоз, болезнь Лайма, бабезиоз и др. Эти заболевания очень часто протекают не самостоятельно, а как коинфекции, так как в их эпидемиологии как векторы принимают участие одни и те же переносчики. Встречается хронический эрлихиоз совместно, например, с лайшманиозом (49%), бабезиозом (4%), гепатозоонозом (10%), чумой (3%). У 85% собак с гепатозоонозом установлены антитела E.canis; доказаны коинфекции и с Ehrlichia platys, Borrelia burgdorferi и Leishmania infantum. Наличие коинфекции является трудной диагностической дилеммой, как для специалистов-практиков, так и для исследователей (Breitschwerdt, 2003).
Лечение
Наиболее часто используемое антимикробное средство для лечения МЭС - это Doxycycline в дозе 5mg/kg за 12 часов. Продолжительность лечения требует не менее 3-х недель (а лучше, - 4 недели). Видимое клиническое улучшение в острой фазе МЭС проявляется через 24-72 часа после начала лечения. И это показывает, что лечение нужно продолжить на протяжении рекомендованного выше времени (Рис.3 и Рис.4). Для лечения МЭС вводили дополнительно Imidocarb dipropionate - 5mg/kg/ i.m. - одна или две аппликации каждые 14 дней. Первоначальные исследования показали хорошую эффективность Имидокарба in vivo, но последующие исследования in vitro не подтвердили это. Однако лечение Имидокарбом оправдано с точки зрения некоторых других инфекций, передающихся кровью (бабезиоз). Необходимо знать, что инъекции Имидокарбом могут вызывать боль. Более того, в течение 10 минут после введения можно ожидать его антихолинэстеразное действие и последующие признаки со стороны парасимпатикуса (слюнотечение, серозные выделения из глаз, рвота, диарея, тремор и одышка, которые обычно исчезают в течение 30 минут).
В качестве поддерживающей терапии при МЭС можно включить глюкокортикоиды. Непродолжительный курс (2-7 дней) лечения Преднизолоном может скорректировать тромбоцитопению. Кроме того, стероиды показаны при лечении артрита, васкулита, менингоэнцефалита и при различных эрлихиозных инфекциях.
Если диагностируется острое течение МЭС и немедленно принимаются меры для лечения, то прогноз может быть благоприятным. Иногда острая фаза без лечения может быть преодолена, и тогда больное животное переходит в субклиническую фазу. В этой фазе прогноз также может быть благоприятным, но следует иметь в виду, что МЭС легко может перейти в хроническую форму, и результат нередко бывает фатальным.
Профилактика
В настоящее время отсутствуют эффективные вакцины, хотя в этом направлении ученые давно работают. Основной профилактической мерой против МЭС остается в настоящее время борьба с векторами. Нужно регулярно использовать ошейники от клещей и Спот Он формы, а также регулировать продолжительность их действий. В эндемических регионах рекомендуются низкие дозы Окситетрациклина - 6.6mg/kg ежедневно. В качестве превентивной меры должен быть введен скрининг доноров крови по отношению к Е.canis, потому что, как известно, эта инфекция может передаваться при переливании крови.
Отношение к людям
В 1996 году впервые установлена инфекция у людей, вызванная Е.canis. Возбудитель культивировали из хронически инфицированных бессимптомных пациентов в штате Лара, Венесуэла (Perez et al.,1996). Выделенный штамм был назван венесуэльским человеческим штаммом Е.canis.
Известно, что Ehrlichia canis очень близок по отношению к антигенам с Ehrlichia chaffeensis – человеческим возбудителем моноцитарного эрлихиоза. Клиническая картина, которую вызывают эти две эрлихии, очень сходна.
В 2002 году в центральную больницу в Ларе, Венесуэла, вновь поступают 20 пациентов с лихорадкой (>390C), головной болью, миалгией, сыпью, болями в суставах и цитопенией (Perez and al, 2006). Пациенты были в возрасте от 13 до 38 лет. У 6 больных (30%) были положительные результаты ПЦР для E.canis (16S rRNA).
Полученные результаты показывают генетическую идентичность с выделенным в 1996 году венесуэльским человеческим штаммом Е.canis. Это первое сообщение о клинически доказанном моноцитарном эрлихиозе у людей возбудителем E. canis.
Литература
1. Цачев Ил. Екзотични зоонози по кучетата в България (моноцитна ерлихиоза, гранулоцитна анаплазмоза, висцерална лайшманиоза): откриване и проучване. Дисертация за доктор на ветеринарномедицинските науки. Тракийски университет, Стара Загора, 315 стр., 2009.
2. Tsachev I. Detection of Antibodies Reactive with Ehrlichia canis in a Kennel in Bulgaria. Turk. J. Vet. Anim. Sci., 30: 425-426. 2006.
3. Tsachev I., Kontos V., Zarkov I. , Krastev S. Survey of antibodies reactive with Ehrlichia canis among dogs in South Bulgaria . Revue de Médecine Vétérinaire, 157, 10: 481-485, 2006.
4. Tsachev I., Papadagjannakis E., Kontos V., Zarkov I., Petrov V., Pelagic V. Seroprevalence of Ehrlichia canis infection among privately-owned dogs in northern Bulgaria. Journal of the Hellenic Veterinary Medical Society, 57 (3): 212-216, 2006.
5. Tsachev. I., Simeonov R., Petrov V. Infections with Ehrlichia canis and Borrelia burgdorferi in a dog. Veterinarski glasnik, 61, 3-4:201-210, 2007.
6. Tsachev I., Ivanov A., Dinev I., Simeonova G., Kanakov D. Clinical Ehrlichia canis and Hepatozoon canis co-infection in a dog in Bulgaria. Revue de Médecine Vétérinaire, 159, 2: 68-73, 2008.




Назад в раздел

















